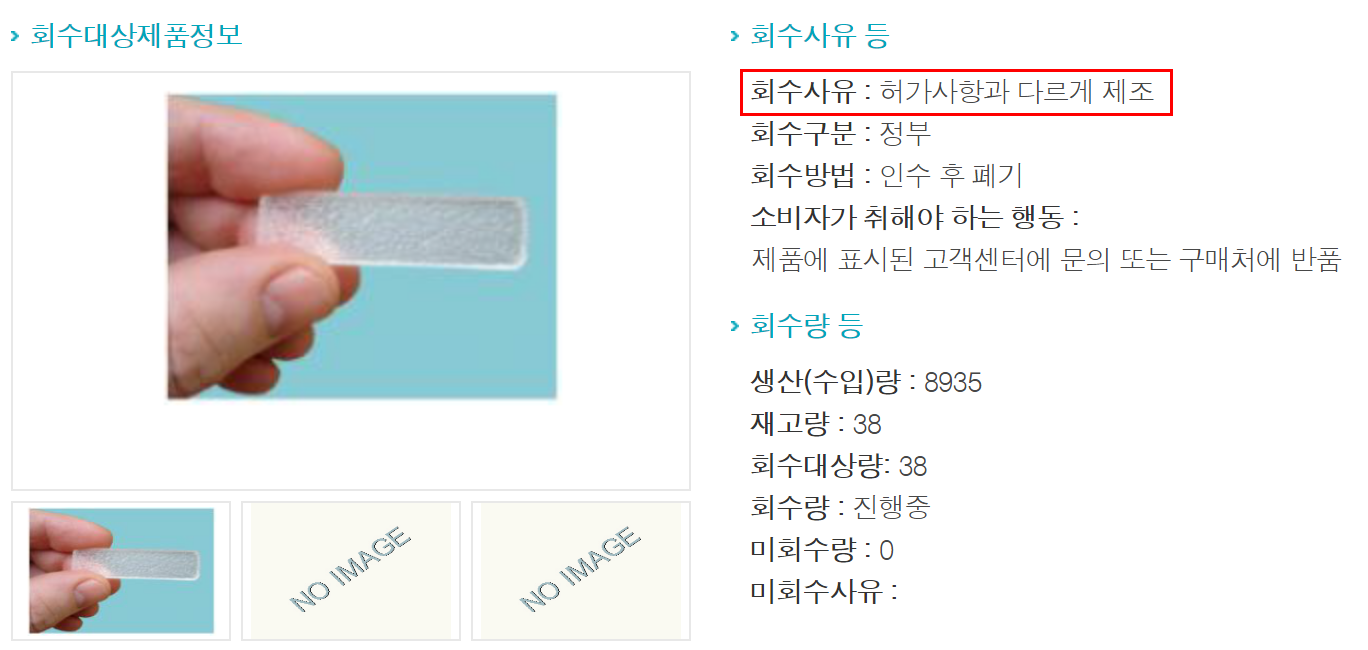

계속된 세포독성 부적합으로 허가 승인을 받기 위한 샘플을 따로 제조(젤라틴 사용)하여 합격 성적서를 발급받았습니다.-2017년 9월 27일, 한스바이오메드 내부 이메일 기록
추후 해당 문제점을 해결하기 위해 다른 실험방법의 세포독성테스트 진행 및 신규허가를 검토하였으나, 원재료(2가지)와 세포독성테스트 면제 사유를 설명할 수 없어 진전이 없는 상태입니다.-2017년 9월 27일, 한스바이오메드 내부 이메일 기록
| 취재 | 홍우람 |
| 디자인 | 이도현 |
| 웹출판 | 허현재 |
뉴스타파는 권력과 자본의 간섭을 받지 않고 진실만을 보도하기 위해, 광고나 협찬 없이 오직 후원회원들의 회비로만 제작됩니다. 월 1만원 후원으로 더 나은 세상을 만들어주세요.